目 录 上一节 下一节 查 找 检 索 手机阅读 总目录 问题反馈
5.4 工艺用水
5.4.1 饮用水的制备和使用应符合下列规定:
1 饮用水的制备方式应保证其水质符合现行国家标准《生活饮用水卫生标准》GB 5749的有关规定;
2 饮用水的储存和输送应符合本标准第10.2.1条和第10.2.2条的规定。
5.4.2 纯化水的制备、储存和分配应符合下列规定:
1 纯化水的制备方式应保证其水质符合现行《中华人民共和国药典》纯化水标准的规定。
2 用于纯化水储存和输送的储罐、管道、管件的材料,应无毒、耐腐蚀、易于消毒,并应采用内壁抛光的优质不锈钢或其他不污染纯化水的材料。储罐的通气口应安装不脱落纤维的疏水性过滤器。
3 纯化水输送管道系统宜采取循环方式。设计和安装时,不应出现使水滞留和不易清洁的死角。循环干管的回水流速不宜小于1m/s,不循环支管长度不宜大于支管管径的3倍。纯化水终端净化装置的设置应靠近使用点。
4 纯化水储存和输送系统应有清洗和消毒措施。
5.4.3 注射用水的制备、储存和使用应符合下列规定:
1 注射用水的制备方式应保证其水质符合现行《中华人民共和国药典》的注射用水标准的规定。
2 用于注射用水储罐和输送管道、管件等的材料应无毒、耐腐蚀、耐高温灭菌,并应采用内壁抛光的优质不锈钢管或其他不污染注射用水的材料。储罐的通气口应安装不脱落纤维的疏水性除菌过滤器。
3 注射用水输送管道系统应采取循环方式。设计和安装时,不应出现使水滞留和不易清洁的死角。循环干管的回水流速不应小于1m/s,循环温度可保持在70℃以上,不循环支管长度不宜大于支管管径的3倍。注射用水终端净化装置的设置应靠近使用点。
4 注射用水储存和输送系统应设置在线清洗、在线消毒设施。
5.4.2 纯化水可直接用于部分药品生产,也是制备注射用水的水源。
1 纯化水的制备方法很多,如蒸馏法、离子交换法、反渗透法等。在确定纯化水制备工艺流程时,应根据药品生产工艺要求,结合当地的水质、供水条件、能源供应、三废处理要求,以及投资控制等因素优化选择,使纯化水质量符合现行《中华人民共和国药典》各项检查指标。
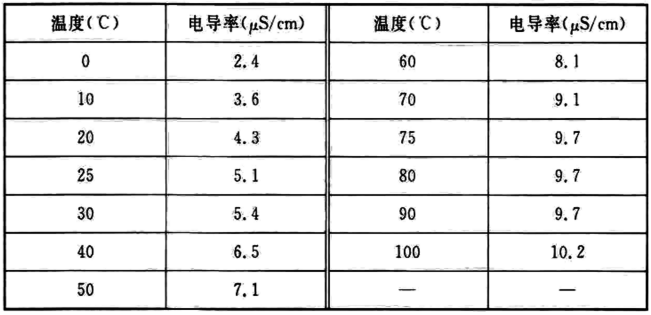
由于原水中所含的氯化物、硫酸盐、硝酸盐、亚硝酸盐等无机盐会影响纯化水的电导率,所以通过对电导率的监测可反映水质的变化情况。原规范规定了电阻率必须大于0.5MΩ·cm的要求,但实际上水的电阻率随着温度的不同而变化,因此本次修订时取消了纯化水的电阻率指标。《中华人民共和国药典》2015版四部通则0681:“制药用水电导率测定法”给出了不同温度下纯化水的电导率,见表3。
表3 不同温度下纯化水的电导率标准
关于纯化水、注射用水的标准,我国药典与美国药典、欧盟药典在电导率(无机杂质控制指标)、总有机碳(有机杂质控制指标)、细菌内毒素、微生物等指标的限度控制方面不尽相同,见表4,对水质和药品质量存在一定影响。为控制水中各种杂质和微生物量,本标准在管网设计,管路的材质、加工、安装、维护等方面做了较多规定。
表4 各国药典纯化水和注射用水标准

2 中国药典对纯化水有“微生物限度”规定,每1mL纯化水中细菌、霉菌和酵母菌总数不得超过100cfu。水系统设备、管道选材不当是造成水污染的主要原因。水系统的微生物污染还会导致纯化水中“细菌内毒素”增加。细菌内毒素又称“热原”,注射后会使患者产生热原反应,严重的会危及生命。细菌内毒素耐热性强,如各种革兰氏阴性菌分离出来的热原,常规灭菌(121℃灭菌30min)对它并无影响,必须加热至180℃、4h才能将它杀灭。因此纯化水储罐和输送管道所用材料应为无毒、耐腐蚀及经得起消毒的材料。
纯化水输送管道的管材选择和管网设计是保证使用点水质的关键。
在纯化水管材选择方面应考虑以下因素:
(1) 材料的化学稳定性:纯化水是一种极好的溶剂,为了保证在输送过程中纯化水水质下降最小,必须选择化学稳定性极好的管材,也就是在所要求的纯化水中的溶出物最少。
(2) 管道内壁的光洁度:管道内壁粗糙,即使微小的凹凸都会造成微粒的沉积和微生物的繁殖,导致微粒和细菌两项指标均不合格。
(3) 管道及管件的接头处的平整度:接头处不平整或垫片尺寸不匹配,会产生水涡流和水滞留,造成微粒的沉积和微生物的繁殖。
如果水系统使用了不适当的材料如PVC,运行后PVC中微量增塑剂会被浸出到水中。采用不锈钢时,要选用焊接良好、内壁抛光的优质不锈钢,并采用自动氩弧焊接,以保证焊接良好、内壁光滑。由于不锈钢管道焊接后焊缝表面金相组织发生变化,导致比未焊接时更易受到腐蚀,同时焊接还会使不锈钢表面粗糙,容易滞留水中的微生物从而形成生物膜,对清洗和灭菌不利,因此焊接后还必须进行钝化处理,以在不锈钢材料表面形成一层致密的氧化膜层,使它在常温下具有抗氧化和耐腐蚀的能力。
不锈钢管道内壁光洁程度以表面粗糙度Ra来衡量。表面粗糙度为0.5μm时可视为光滑,粗糙度为0.25μm时可视为镜面程度。世界卫生组织(WHO)《药品生产质量管理规范》附录3“制药用水”中规定制药用水管道如采用不锈钢,其材料级别必须为316,管道抛光后的内表面的粗糙度的算术平均值(Ra)不得超过0.8μm[美国机械工程师协会生物工程设备(ASME BPE)2014规定Ra小于或等于0.6μm]。抛光可采用机械抛光或电抛光,而后者有利于改善不锈钢材料表面的抗腐蚀性。
纯化水储罐的通气口是外界含尘、含菌空气侵入水系统的主要途径,因此必须安装效果确切的疏水性呼吸过滤器以防大气中的尘粒、细菌的倒灌。
3 为防止纯化水在输送过程中或静止状态受到微生物的污染,纯化水的输送宜采用循环供水管道系统,并需保持一定的流速,使水流呈湍流状态(雷诺数Re>10000),以防止管壁形成微生物生物膜。生物膜是某些微生物应变的结果,它能保护微生物,一般的消毒剂很难将它杀灭,它的脱落便成了新的菌落。
管路设计安装时要保持坡度,以利于放净剩水。还应避免出现使水滞留和不易清洗的部位。管道的某些部位流量过低,微生物在这些管道表面、阀门和其他区域容易形成生物膜,成为持久性的污染源。生物膜很难消除,最好是防止它的生成。
4 纯化水储罐和输水系统的定期清洗是保证纯化水水质的重要手段,防止长期运行后,储罐和管道内壁产生沉积物及微生物积聚,使水质下降。纯化水储罐常用的消毒方式有臭氧消毒法和巴氏消毒法,也可使用饱和蒸汽消毒。如采用后者,则纯化水储罐必须耐压,不要使用不耐压且不宜放尽的平底储罐。
5.4.3 注射用水常用于无菌药品的配料、直接接触无菌药品的包材、器具的最后淋洗以及作为灭菌注射用水的原料等。
1 注射用水的制备可采用蒸馏法、反渗透法和超滤法。由于反渗透法、超滤法均存在一定的缺陷,因此蒸馏法是中国药典确认的唯一制备方式。蒸馏法以纯化水作为原料,通过蒸发、汽液分离、冷凝等过程,去除水中的化学物质、微生物及细菌内毒素,以达到现行《中华人民共和国药典》注射用水的标准。
2 为保证注射用水在储存、输送的过程中不受到二次污染,对储罐、输送管道及管件的材质有特殊的要求,必须使用无毒、耐腐蚀、可消毒灭菌,内壁抛光的优质不锈钢(如316L不锈钢)或其他不污染注射用水的材料。使用不锈钢材料时,要求采用内壁抛光的不锈钢管,并采用自动氩弧焊接,以保证焊接良好、内壁光滑。由于不锈钢管道焊接后焊缝表面金相组织发生变化,导致比未焊接时更易受到腐蚀,同时焊接还会使不锈钢表面粗糙,容易滞留水中微生物形成生物膜,对清洗和灭菌不利,因此焊接后还必须进行钝化处理,以在不锈钢材料表面形成一层致密的氧化膜层,使它在常温下具有抗氧化和耐腐蚀的能力。
注射用水储罐的通气口是外界含尘、含菌空气侵入注射用水系统的主要途径。因此,储罐的通气口必须安装0.22μm疏水性呼吸过滤器,防止微粒和微生物的侵入。
3 为防止储存的注射用水受微生物污染,注射用水可采用70℃以上保温循环的方式。原规范根据我国1998年版药品GMP的规定,储存方式包括80℃以上保温储存和65℃以上或4℃以下保温循环的方式。根据使用经验,较高的储存温度也是不锈钢表面形成“红锈”的原因之一。故此次修订时,参照我国药品GMP(2010年修订)关于注射用水的条款,确定了70℃以上保温循环的方式。药品生产企业可根据生产工艺要求和风险管理原则,通过验证自行确定注射用水的保存方式。
为防止注射用水在输送或静止状态受到微生物污染,注射用水输送系统应采用循环供水方式,循环干管应保持一定的流速,使水流呈湍流状态(雷诺数Re>10000),以免微生物的再生和细菌内毒素的形成。原规范中规定循环主管水的流速不小于1.5m/s,没有考虑到用水量的变化情况。当循环回路中有大用水量点时(如安瓿洗瓶机),使用点后的流量会降低,从而造成流速下降。比较有效的办法是控制循环系统末端的回水流速,从而保证整个循环回路中具有一定的流量,防止水流过慢。《国际制药工程协会(ISPE)制药用水指南》中规定了此流速不应低于3ft/s,本标准据此提出了循环系统管道末端的回水流速不应小于1m/s。另外,注射用水系统设计及安装时要严格保持坡度,避免出现水滞留及不易清洗的盲管,要求在水系统灭菌前能将管道中的剩水放尽,确保灭菌效果。
关于循环系统中不循环支管段的长度问题,目前有不同的标准。原规范中规定不大于6倍,源自《国际制药工程协会(ISPE)制药用水指南》,且其支管长度从主管中心开始计算。而《美国机械工程师协会“生物加工设备”(ASME BPE)2014》中规定,L/D≯2,其中L为从循环主管边计算的非循环支管长度(如有阀门则到阀门密封面),D为非循环支管的长度。根据制药行业实际经验,L/D≯3,同时保持循环系统水的湍流状态,可有效避免支管中水的滞留问题,因此本标准修订时采用了不循环支管长度不超过支管直径3倍的标准,且长度从循环主管壁计算至支管阀门密封面,如图1所示。
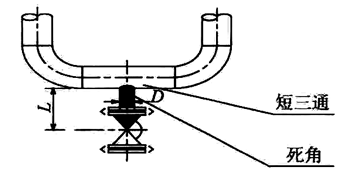
图1 纯化水、注射用水使用点支管长度示意图
实际使用时,对于支管管径较小(如DN15)的使用点,由于阀门结构原因,L/D≯3较难满足。此时可考虑采用零死角的U形弯和阀门组件,或加大支管管径以满足要求。
说明 返回
顶部
目录导航
- 前言
- 1 总则
- 2 术语
- 3 生产区域的环境参数
- 3.1 一般规定
- 3.2 环境参数的设计要求
- 4 厂址选择和总平面布置
- 4.1 厂址选择
- 4.2 总平面布置
- 5 工艺设计
- 5.1 工艺布局
- 5.2 人员净化
- 5.3 物料净化
- 5.4 工艺用水
- 6 工艺管道
- 6.1 一般规定
- 6.2 管道材料、阀门和附件
- 6.3 管道的安装、保温
- 6.4 安全技术
- 7 工艺设备
- 7.1 一般规定
- 7.2 设计和选用
- 8 建筑设计
- 8.1 一般规定
- 8.2 防火和疏散
- 8.3 室内装修
- 9 空气净化
- 9.1 一般规定
- 9.2 净化空气调节系统
- 9.3 气流流型和送风量
- 9.4 风管和附件
- 9.5 监测与控制
- 9.6 生产特殊性质药品医药洁净室的要求
- 10 给水排水
- 10.1 一般规定
- 10.2 给水
- 10.3 排水
- 10.4 消防设施
- 11 电气设计
- 11.1 配电
- 11.2 照明
- 11.3 通信
- 11.4 静电防护及接地
- 附录A 药品生产环境的空气洁净度级别举例
- 附录B 医药洁净室的维护管理
- 附录C 医药洁净室的验证
- 本标准用词说明
- 引用标准名录
-
笔记需登录后才能查看哦~


 京公网安备110105014475
京公网安备110105014475